A cura di Tanja Bagar

La dottoressa Tanja Bagar è una microbiologa con un dottorato in biomedicina. Ha acquisito una vasta esperienza di ricerca sulla biotecnologia, sulla biologia molecolare e sulla segnalazione cellulare in laboratori in Slovenia, Germania e Regno Unito. La sua attenzione si è concentrata principalmente sul sistema endocannabinoide e sui principi attivi della cannabis/canapa. Il suo lavoro ha portato alla formazione dell'Istituto Internazionale per i Cannabinoidi (ICANNA), di cui è l'amministratore delegato e presidente del comitato scientifico. È anche vicedirettrice e capo della R&S in una società ambientale. La dott.ssa Bagar è anche attiva nella sfera accademica. È docente di microbiologia e preside del programma di master in Ecoremediations presso la facoltà Alma Mater Europaea.
Il SEC e il metabolismo
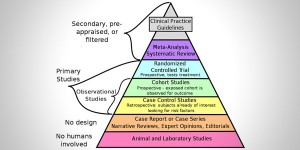
Man mano che impariamo sempre di più sul sistema endocannabinoide, diventa sempre più evidente che la definizione ristretta di questo sistema non si applica più, né descrive accuratamente la complessità di questo sistema di regolazione. Sappiamo che il nostro corpo produce molti endocannabinoidi, che abbiamo più di due recettori di cannabinoidi e che i fitocannabinoidi hanno molti obiettivi molecolari nelle nostre cellule e tessuti. Di conseguenza, alcuni autori usano ora una definizione estesa del sistema endocannabinoide, come "sistema endocannabinoide allargato o espanso" o semplicemente "endocannabinoidoma". Questo termine rappresenta l'insieme degli endocannabinoidi, dei mediatori simili agli endocannabinoidi e dei loro numerosi recettori ed enzimi metabolici.
L'endocannabinoidoma è coinvolto nel controllo di molti processi nel nostro corpo e il ruolo di questo sistema è molto complesso. Esso influisce sulla maggior parte dei sistemi fisiologici, e i recettori dei cannabinoidi sono espressi (in densità diverse) in tutti i tipi di cellule studiate. Quindi, descrivere cosa fa esattamente non è un compito facile, in quanto regola la biochimica della maggior parte dei 37 trilioni di cellule del nostro corpo. La ricerca ha dimostrato che il sistema endocannabinoide funziona come un meccanismo di SOS che si attiva ogni volta che il nostro corpo è fuori equilibrio per qualsiasi motivo. Per esempio, si attiva quando soffriamo di una lesione fisica, quando incontriamo microbi patogeni e anche quando sentiamo dolore emotivo o siamo sotto stress. Sembra che il SEC serva come meccanismo protettivo generale, a partire dal livello cellulare e procedendo verso i tessuti, gli organi, il corpo e il nostro benessere generale.
Non c'è da stupirsi che l'endocannabinoidoma sia coinvolto in tutti gli aspetti del nostro metabolismo, compresi l'appetito, l'equilibrio energetico, il metabolismo, la termogenesi, l'infiammazione, la nocicezione e la regolazione dello stress, delle ricompense e delle emozioni. Poiché la prevalenza dei disturbi metabolici, tra cui l'obesità, è in costante aumento, gli scienziati sono alla ricerca di nuove strategie terapeutiche che includano il SEC espanso. I componenti dell'endocannabinoidoma stanno emergendo come potenti obiettivi terapeutici a causa del loro ruolo nella regolazione del consumo di cibo e dell'equilibrio energetico, nonché il metabolismo dei lipidi e del glucosio. Gli studi hanno dimostrato che il SEC è sovraregolato nell'obesità e nei disturbi metabolici associati. I livelli di endocannabinoidi sono elevati negli individui obesi rispetto ai magri. L'aumento della concentrazione di endocannabinoidi è stato dimostrato al livello di sistema nervoso centrale, tessuto adiposo, pancreas, di sistema muscolo-scheletrico, nei reni, nel fegato e nel sangue di roditori e umani obesi. La causa non è molto chiara, ma potrebbe essere dovuta a una maggiore sintesi di endocannabinoidi o a una loro ridotta degradazione, nonché a una sovraespressione dei recettori dei cannabinoidi. Diversi studi hanno dimostrato livelli sovraregolati di 2-AG in diversi organi e nel siero durante l'obesità e l'iperglicemia correlata al contenuto di grasso corporeo, alla massa di grasso viscerale e alle concentrazioni di triacilgliceridi e insulina nel plasma a digiuno. Allo stesso modo, diversi studi hanno rivelato un'associazione sostanziale tra il livello di AEA e l'indice di massa corporea (BMI).
L'attivazione del recettore CB1 è coinvolta nel controllo del metabolismo dei lipidi e del glucosio. Anche se il CB1 è principalmente espresso nel sistema nervoso e i suoi livelli di espressione sono bassi nelle cellule periferiche, essi aumentano in caso di obesità. Il blocco del CB1 riduce l'assunzione di cibo e il peso corporeo. Con questo in mente, Rimonabant, un antagonista al CB1, era stato sviluppato e prescritto come farmaco anti-obesità, ma aveva gravi effetti collaterali tra cui depressione, ansia, nausea vertigini e suicidalità probabilmente a causa del blocco del CB1 centrale. Ci sono notevoli prove sull'impatto negativo che il CB1 ha sulla termogenesi. È stato osservato che i topi privi di CB1 hanno meno grasso e sono più protetti contro l'obesità rispetto ai corrispondenti topi non modificati. Il recettore CB1 è noto per i suoi effetti di stimolazione dell'appetito dovuti al legame del THC a questo recettore, che producono la cosiddetta fame chimica. Gli effetti di stimolazione dell'appetito della cannabis sono noti da molto tempo, con fonti storiche che indicano che già nel 300 a.C. si sapeva che la cannabis stimolava l'appetito, specialmente per il cibo dolce e salato. Anche il CB2 gioca un ruolo nell'alimentazione; in particolare i suoi agonisti possono ridurre l'assunzione di cibo.
Tessuto adiposo
I disordini metabolici, tra cui la resistenza all'insulina e l'obesità, sono gravi problemi di salute emergenti a livello mondiale. Queste condizioni sono caratterizzate da un accumulo di grasso eccessivo o anomalo, il cosiddetto tessuto adiposo, e sono importanti fattori di rischio per una serie di malattie croniche, come le malattie cardiovascolari e il diabete, e in generale causano una peggiore qualità della vita.
Il tessuto adiposo è comunemente distinto in tessuto adiposo bianco e bruno, sulla base del suo aspetto. Il tessuto adiposo bruno (BAT) è caratterizzato da piccole gocce lipidiche e da un'alta densità di mitocondri, che portano all'aspetto bruno. Le cellule del tessuto adiposo bianco (WAT) di solito mostrano solo una goccia di lipidi. Le differenze morfologiche riflettono anche funzioni diverse. Il BAT è coinvolto nella termogenesi e nel dispendio calorico durante il riposo e l'esercizio. Il WAT è coinvolto nello stoccaggio del grasso e nella secrezione endocrina di ormoni. In risposta a vari stimoli, il tessuto adiposo bianco può iniziare a mostrare le caratteristiche delle cellule adipose brune, che sono chiamate adipociti beige o brite.
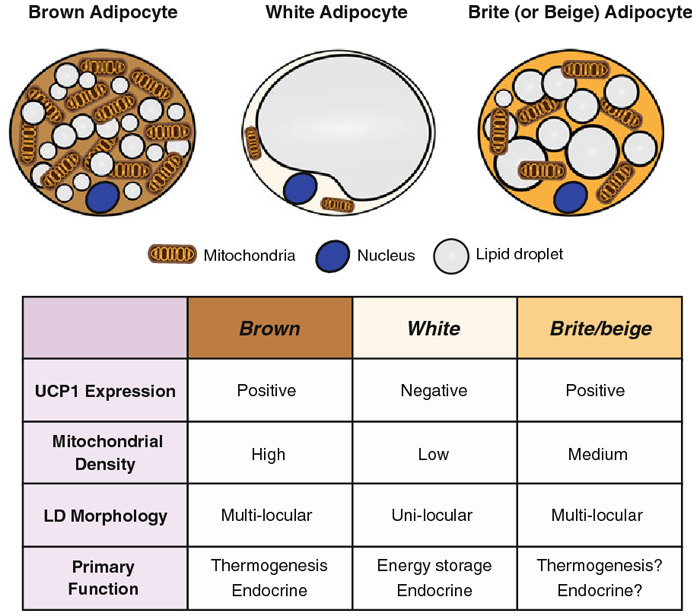
Fonte della foto: Jung et al., 2019
| Adipocita Bruno | Adipocita bianco | Adipocita brite (o beige) |
| Mitocondri | Nucleo | Goccia lipidica |
| Bruno | Bianco | Brite / beige | |
| Espressione UCP1 | Positiva | Negativa | Positiva |
| Densità mitocondriale | Alta | Bassa | Media |
| Morfologia LD | Multiloculare | Uniloculare | Multiloculare |
| Funzione primaria | Termogenesi
Endocrina |
Stoccaggio energia
Endocrina |
Termogenesi?
Endocrina? |
Sempre più ricerche dimostrano che l'induzione o il reclutamento di adipociti beige o brite, insieme all'attivazione del BAT, potrebbero proteggere dall'obesità. L'attività del BAT ha il potenziale di influenzare significativamente il peso corporeo, il metabolismo del glucosio e dei lipidi. Esso è coinvolto nella dissipazione dell'energia come calore, grazie a una speciale proteina chiamata UCP1 sulla membrana interna dei mitocondri. Gli adipociti bruni sembrano essere responsabili di una grande produzione di calore, significativamente più alta che in altri organi, aumentando così il dispendio energetico del corpo. Diversi attivatori sono stati associati all'imbrunimento del WAT, come l'esposizione al freddo, l'esercizio, gli ormoni tiroidei, le catecolamine, la capsaicina ecc. La conversione del WAT in tessuto adiposo beige è un potenziale nuovo bersaglio terapeutico per l'obesità.
I tessuti adiposi esprimono entrambi i recettori dei cannabinoidi, la cui attivazione influenza significativamente l'attività metabolica delle cellule adipose. Il blocco del recettore CB1 ha dimostrato di indurre la differenziazione degli adipociti bianchi verso un fenotipo termogenico delle cellule brune, che è altamente vantaggioso quando vogliamo ridurre il tessuto adiposo. Gli effetti del recettore CB2 sull'obesità sono poco conosciuti, ma sappiamo che è fortemente coinvolto nell'omeostasi energetica. È stato dimostrato che l'attivazione del CB2 induce la generazione di calore con conseguente dispendio energetico nel tessuto adiposo e che la stimolazione cronica del CB2 attenua l'aumento di peso corporeo. Pertanto il CB2 sembra un bersaglio promettente nell'obesità in quanto dovrebbe facilitare gli effetti anti-obesità senza esercitare un'attività psicotropa a livello centrale.
Tetraidrocannabinolo (THC)
Il THC è un agonista parziale dei recettori CB1 e CB2 ed è il costituente psicoattivo della cannabis, grazie al suo legame con il recettore CB1 nel cervello. Inoltre, il THC attiva i recettori CB1, situati nella regione limbica (aumentando le proprietà motivazionali del cibo) e ipotalamica (aumentando l'appetito) del cervello, causando una stimolazione acuta dell'appetito – i cosiddetti effetti orexigenici. D'altra parte è stato dimostrato che ha un potenziale effetto anti-obesità. In un modello in vivo i ricercatori hanno dimostrato che la somministrazione cronica di THC a topi con obesità indotta dalla dieta (DIO) per 3 e 4 settimane di trattamento ha impedito l'aumento di peso a causa di una ridotta assunzione di energia. È stato anche riportato che il THC ha un impatto benefico sulla regolazione della sensibilità all'insulina negli adipociti resistenti all'insulina. I meccanismi o questi doppi effetti non sono completamente chiariti, ma poiché il THC non produce una stimolazione massima dei recettori CB1, una spiegazione potrebbe essere che gli effetti anti-obesità osservati potrebbero derivare dal fatto che impedisce all'agonista completo, l'anandamide, di legarsi al recettore CB1, soprattutto perché il tono endocannabinoide nelle persone obese è alto. Tuttavia, la potenziale influenza positiva del THC nella prevenzione e nel trattamento dell'obesità richiede ulteriori indagini.
Tetraidrocannabivarina (THCV)
La THCV si lega a entrambi i recettori CB1 e CB2 dei cannabinoidi. La sua azione sembra essere dipendente dalla dose, poiché la THCV a basse dosi è un antagonista neutro, e ad alte dosi un agonista dei recettori CB1 e CB2. Avendo un'azione antagonista del CB1, sembrava essere un candidato promettente per i disturbi metabolici e l'obesità. La ricerca ha confermato questo in parte, poiché la THCV ha dimostrato di avere un potenziale effetto terapeutico nel trattamento del diabete associato all'obesità. La THCV ha aumentato la sensibilità all'insulina e migliorato la tolleranza al glucosio in topi con obesità indotta dalla dieta e in topi con obesità indotta geneticamente. La THCV ripristina inoltre la via di segnalazione intracellulare dell'insulina e diminuisce l'accumulo di lipidi nel fegato e negli adipociti. Uno studio pilota in pazienti con diabete di tipo 2 ha mostrato che la THCV ha ridotto il glucosio plasmatico a digiuno con un miglioramento parallelo della funzione delle cellule β nel pancreas. Quindi questo fitocannabinoide dovrebbe essere fortemente considerato quando si devono affrontare disturbi metabolici.
Cannabidiolo (CBD)
Il CBD ha una vasta gamma di effetti farmacologici ben studiati attraverso numerosi meccanismi diversi. È un modulatore allosterico negativo del recettore CB1, che ne blocca il legame con un forte agonista come l'anandamide, producendo così effetti anti-obesità. Poiché nell'obesità il SEC è iperattivo, c'è un eccesso di anandamide e 2-AG, che causa un'iperattivazione del recettore CB1. Al recettore CB2 può agire come agonista o agonista inverso a seconda della dose e del modello di ricerca. Il CBD ha anche affinità per vari altri recettori, tra cui GPR55, gli α1-adrenorecettori, 5-HT1A (serotonina), canali TRPV e PPARγ. Il CBD mostra molte proprietà terapeutiche, tra cui effetti antinfiammatori, antiossidanti, antitumorali, anticonvulsivanti e neuroprotettivi. Per questo motivo il CBD emerge come un potenziale agente terapeutico, che può essere utilizzato nel trattamento del diabete e delle sue complicanze, di obesità, ischemia, malattie neurodegenerative così come nella terapia del dolore e della depressione. Poiché l'obesità è associata a un'infiammazione cronica di basso livello, il CBD può giocare un ruolo cruciale nel ridurre questa risposta infiammatoria e favorire una massa corporea più sana. A questo proposito, il CBD è stato ampiamente studiato e ha dimostrato di aumentare il livello di glutatione (GSH), adenosina trifosfato (ATP), e nicotinamide adenina dinucleotide (NAD), aumentando la lipolisi intracellulare e l'attività mitocondriale (36). Il CBD ha molti effetti benefici sul fegato, un organo chiave in tutti i processi metabolici e nell'equilibrio energetico, poiché attenua la steatosi epatica (diminuzione dell'accumulo di triacilgliceridi e gocce di grasso), la risposta infiammatoria, lo stress nitrativo, la ridotta perossidazione lipidica, l'espressione di specie reattive dell'ossigeno e l'infiltrazione di neutrofili nel fegato. Gli effetti del CBD sull'assunzione di cibo, sulle preferenze alimentari e sull'aumento di peso sono meno chiari e hanno mostrato una serie di risultati contraddittori. Uno studio ha dimostrato che il CBD ha causato una diminuzione dell'aumento di peso corporeo nei ratti, mentre altri studi su ratti e topi non hanno mostrato alcun impatto significativo sull'assunzione di cibo e sul peso corporeo. Uno studio ha anche dimostrato che il CBD in ratti alimentati con una dieta ad alto contenuto di grassi ha provocato un aumento del peso corporeo nonostante una assunzione significativamente ridotta di cibo. Indipendentemente dai risultati contraddittori del CBD sull'alimentazione, il CBD mostra molteplici effetti benefici su diversi tipi di cambiamenti e patologie coinvolte nell'obesità. Poiché si lega a molti recettori, esso produce effetti su molti organi cruciali nel metabolismo, come il fegato, il tessuto adiposo, il pancreas e il cuore. È interessante notare che ha anche causato cambiamenti rilevanti in ormoni intestinali come il GIP - peptide insulinotropo glucosio-dipendente - e le concentrazioni di adipochine.

Fonte della foto Bielawiec et al., 2020
| CBD | |||
| CB1, CB2 | TRPV | GPR55 | |
| Tessuti | |||
| Fegato | Cuore | Tessuto adiposo | Pancreas endocrino |
| ↑ Lipolisi | ↓ Fibrosi cardiaca | ↑ Lipolisi | ↑ Utilizzo di energia |
| ↑ Attività mitocondriale | ↓ Stress ossidativo | ↑ Assorbimento di glucosio | ↓ TNF-α, IFN-γ, COX |
| ↑ AMPKa2 | ↓ Infiammazione | ↑ Attività mitocondriale | ↑ NO, PGE |
| ↑ ERK1/2 | ↓ Morte cellulare | ↑ PGC-1α, PPARγ | ↑ IL-4, IL-10 |
| ↑ STAT | |||
Conclusioni
La co-morbilità legata all'obesità è in aumento, ha un costo elevato per la società e riduce la qualità di vita del paziente. Recenti scoperte nel campo dell'imbrunimento del tessuto adiposo bianco (trasformazione da WAT a BAT) hanno evidenziato il ruolo potenziale di questo fenomeno nel trattamento dell'obesità. L'attività del BAT è stata associata a un miglioramento del profilo metabolico negli adulti. L'attivazione del CB2 nella velocizzazione dell'imbrunimento e nella trasformazione dell'energia chimica in energia termica potrebbe essere un pezzo importante del puzzle.
Agire sul CB1 è anche importante, ma sempre tenendo a mente le esperienze con Rimonabant, antagonista del recettore CB1 che è apparso come un promettente farmaco anti-obesità durante gli studi clinici, ma ha anche mostrato importanti effetti collaterali psichiatrici e ha dovuto essere ritirato dal mercato. L'interruzione della sperimentazione clinica relativa all'inibitore FAAH a causa del verificarsi di gravi eventi avversi ha anche dimostrato che l'intervento su questo fondamentale sistema protettivo deve essere fatto con molta attenzione. Qui ancora una volta i fitocannabinoidi mostrano un immenso potenziale, come anche altri ligandi con i recettori dei cannabinoidi dal mondo vegetale. L'obiettivo è trovare antagonisti del recettore CB1 e agonisti del recettore CB2 nel mondo vegetale. Essi mostrano un alto profilo di sicurezza con effetti collaterali trascurabili e hanno obiettivi multipli all'interno dell'endocannabidioma che supportano il metabolismo sano, il dispendio energetico, l'omeostasi biochimica e il benessere emotivo.
Riferimenti
Jung SM, Sanchez-Gurmaches J, Guertin DA. Brown Adipose Tissue Development and Metabolism. Handb Exp Pharmacol. 2019;251:3-36. doi: 10.1007/164_2018_168. PMID: 30203328; PMCID: PMC7330484.
Bielawiec P, Harasim-Symbor E, Chabowski A. Phytocannabinoids: Useful Drugs for the Treatment of Obesity? Special Focus on Cannabidiol. Front Endocrinol (Lausanne). 2020 Mar 4;11:114. doi: 10.3389/fendo.2020.00114. PMID: 32194509; PMCID: PMC7064444.
Rossi F, Punzo F, Umano GR, Argenziano M, Miraglia Del Giudice E. Role of Cannabinoids in Obesity. Int J Mol Sci. 2018 Sep 10;19(9):2690. doi: 10.3390/ijms19092690. PMID: 30201891; PMCID: PMC6163475.
Borowska M, Czarnywojtek A, Sawicka-Gutaj N, Woliński K, Płazińska MT, Mikołajczak P, Ruchała M. The effects of cannabinoids on the endocrine system. Endokrynol Pol. 2018;69(6):705-719. doi: 10.5603/EP.a2018.0072. PMID: 30618031.
Kaur R, Ambwani SR, Singh S. Endocannabinoid System: A Multi-Facet Therapeutic Target. Curr Clin Pharmacol. 2016;11(2):110-7. doi: 10.2174/1574884711666160418105339. PMID: 27086601.
Behl T, Chadha S, Sachdeva M, Sehgal A, Kumar A, Dhruv, Venkatachalam T, Hafeez A, Aleya L, Arora S, Batiha GE, Nijhawan P, Bungau S. Understanding the possible role of endocannabinoid system in obesity. Prostaglandins Other Lipid Mediat. 2021 Feb;152:106520. doi: 10.1016/j.prostaglandins.2020.106520. Epub 2020 Nov 26. PMID: 33249225.
Abioye A, Ayodele O, Marinkovic A, Patidar R, Akinwekomi A, Sanyaolu A. Δ9-Tetrahydrocannabivarin (THCV): a commentary on potential therapeutic benefit for the management of obesity and diabetes. J Cannabis Res. 2020 Jan 31;2(1):6. doi: 10.1186/s42238-020-0016-7. PMID: 33526143; PMCID: PMC7819335.