Par Tanja Bagar

Le Dr Tanja Bagar est une microbiologiste titulaire d'un doctorat en biomédecine. Elle a acquis une vaste expérience de la recherche en biotechnologie, en biologie moléculaire et en signalisation cellulaire dans des laboratoires en Slovénie, en Allemagne et au Royaume-Uni. Elle s'est principalement concentrée sur le système endocannabinoïde et les substances actives du cannabis/chanvre. Ses travaux ont conduit à la création de l'Institut international des cannabinoïdes (ICANNA), dont elle est directrice générale et présidente du conseil d'experts. Elle est également directrice adjointe et responsable de la R&D dans une société environnementale. Elle est également active dans la sphère universitaire. Elle donne des conférences dans le domaine de la microbiologie et est la doyenne du programme de maîtrise en écomédiation de la faculté Alma Mater Europaea.
Le SEC et le métabolisme
À mesure que nos connaissances sur le système endocannabinoïde (SEC) s'élargissent, il devient de plus en plus évident que sa définition étroite ne convient plus ou ne décrit plus avec exactitude la complexité de ce système de régulation. Nous savons que l'organisme produit de nombreux endocannabinoïdes, qu'il compte plus de deux récepteurs des cannabinoïdes et que les phytocannabinoïdes ont plusieurs cibles moléculaires dans nos cellules et tissus. Par conséquent, certains chercheurs et auteurs utilisent maintenant une définition élargie du SEC, soit le « système endocannabinoïde étendu » ou simplement l'« endocannabinoïdome ». Ces termes représentent l'ensemble des endocannabinoïdes, des transmetteurs analogues des endocannabinoïdes ainsi que leurs nombreux récepteurs et enzymes métaboliques.
L'endocannabinoïdome participe au contrôle de plusieurs processus dans l'organisme, son rôle étant somme toute très complexe. Il influe sur la majorité des systèmes physiologiques, et les récepteurs des cannabinoïdes s'expriment (selon différentes densités) sur tous les types de cellules étudiés. Définir son action avec exactitude n'est donc pas une mince tâche, car il régule la biochimie de la grande majorité des 37 billions de cellules de notre corps. Des études montrent que le système endocannabinoïde fonctionne comme un mécanisme de secours qui s'active dès que l'organisme est déséquilibré pour une raison ou une autre. Par exemple, il s'active quand nous souffrons d'une blessure physique, quand nous faisons face à des microbes pathologiques et quand nous ressentons une douleur émotionnelle ou du stress. Le SEC servirait de mécanisme de protection général, d'abord à l'échelle cellulaire, puis sur les tissus, les organes, l'organisme et le bien-être global.
Sans grande surprise, l'endocannabinoïdome joue un rôle dans tous les aspects de notre métabolisme, dont l'appétit, l'équilibre énergétique, le métabolisme, la thermogenèse, l'inflammation, la nociception ainsi que la régulation du stress, du processus de récompense et des émotions. Dans le contexte où la prévalence des troubles métaboliques, y compris l'obésité, est en constante augmentation, les chercheurs se penchent sur de nouvelles stratégies thérapeutiques, notamment liées au SEC étendu. Les composants de l'endocannabinoïdome apparaissent comme de puissantes cibles thérapeutiques en raison de leur rôle dans la régulation de la consommation alimentaire, de l'équilibre énergétique et du métabolisme lipidique et glucidique. Des études ont montré que le SEC est régulé à la hausse en cas d'obésité et de troubles métaboliques connexes. Le niveau d'endocannabinoïdes est plus élevé chez les personnes obèses que les personnes minces. On a observé une concentration plus élevée d'endocannabinoïdes dans le système nerveux central, les tissus adipeux, le pancréas, les muscles squelettiques, les reins, le foie et le sang de rongeurs et de personnes obèses. La cause de ce phénomène reste floue, mais on pourrait l'expliquer par une hausse de la synthèse des endocannabinoïdes ou une diminution de leur dégradation ainsi que par une surexpression des récepteurs des cannabinoïdes. Diverses études ont fait état d'une régulation à la hausse du 2-arachidonylglycérol (2-AG) dans différents organes et dans le sérum en cas d'obésité et d'hyperglycémie, qui était corrélée à la teneur en graisse corporelle, à la masse de la graisse viscérale ainsi qu'aux taux de triglycérides plasmatiques et d'insuline à jeun. De même, plusieurs études ont révélé une association significative entre le taux d'anandamide (AEA) et la valeur de l'indice de masse corporelle (IMC).
L'activation du récepteur CB1 participe au contrôle du métabolisme des lipides et du glucose. Bien que le CB1 s'exprime principalement dans le système nerveux et que son expression soit faible dans les cellules périphériques, celle-ci augmente dans les cas d'obésité. Le blocage du CB1 réduit la prise alimentaire et le poids corporel. Dans cette optique, le Rimonabant, un antagoniste du CB1, a été conçu et prescrit comme médicament contre l'obésité. Il a cependant causé des effets secondaires graves comme de la dépression, de l'anxiété, des nausées, des étourdissements et des tendances suicidaires, probablement en raison du blocage des CB1 centraux. De nombreuses données probantes montrent l'effet négatif du CB1 sur la thermogenèse. Il a été observé que des souris présentant un manque de CB1 ont moins de gras et sont plus protégées contre l'obésité que des souris sauvages correspondantes. Le récepteur CB1 est connu pour ses effets stimulants sur l'appétit puisque le THC s'y lie, ce qui entraîne les fameuses fringales. On connaît depuis longtemps les effets du cannabis sur l'augmentation de l'appétit. Des sources historiques laissent penser que les gens savaient que le cannabis augmentait l'appétit, particulièrement pour les aliments sucrés et salés, aussitôt que 300 AEC. Le CB2 joue aussi un rôle dans l'alimentation; ses agonistes, en particulier, peuvent réduire la prise alimentaire.
Tissu adipeux
Les troubles métaboliques, dont l'insulinorésistance et l'obésité, sont en train de devenir les plus grandes préoccupations en matière de santé partout dans le monde. Ces affections sont caractérisées par une accumulation excessive ou anormale de graisse, soit le tissu adipeux, et représentent un facteur de risque majeur d'un bon nombre de maladies chroniques telles que les maladies cardiovasculaires et le diabète, ainsi que d'une plus faible qualité de vie.
On distingue couramment deux types de tissu adipeux : le blanc et le brun, selon l'apparence. Le tissu adipeux brun (TABr) se caractérise par des gouttelettes de lipides et une haute densité de mitochondries, ce qui lui confère son apparence brunâtre. Les cellules de tissu adipeux blanc (TAB) n'ont habituellement qu'une seule gouttelette de lipides. Ces différences morphologiques reflètent également différentes fonctions. Le TABr participe à la thermogenèse et à la dépense calorique au repos et à l'effort. Le TAB contribue au stockage des graisses et à la sécrétion endocrinienne d'hormones. En réponse à divers stimuli, le TAB peut commencer à montrer des caractéristiques de cellules de tissu adipeux brun : on les appelle alors les adipocytes beiges ou « brite » (une contraction des adjectifs anglais brown et white).
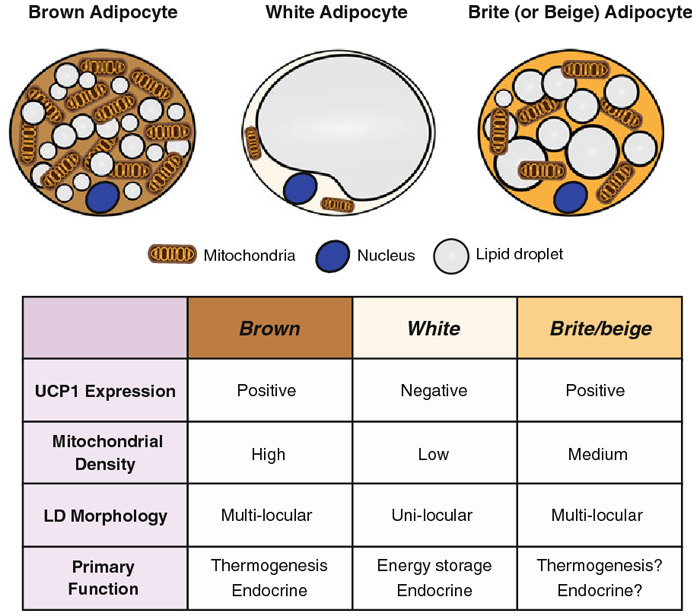
Source de la photo : Jung et coll., 2019
| Adipocyte brun | Adipocyte blanc | Adipocyte beige (ou « brite ») |
| Mitochondrie | Noyau | Gouttelette de lipide |
| Brun | Blanc | Beige/« brite » | |
| Expression de l'UCP1 | Positive | Négative | Positive |
| Densité mitochondriale | Élevée | Faible | Moyenne |
| Morphologie des gouttelettes de lipides | Multiloculaire | Uniloculaire | Multiloculaire |
| Fonction principale | Thermogenèse
Fonction endocrinienne |
Stockage d'énergie
Fonction endocrinienne |
Thermogenèse?
Fonction endocrinienne? |
De plus en plus d'études montrent que l'induction ou le recrutement des adipocytes beiges ou « brite », de concert avec l'activation du TABr, aurait un effet protecteur contre l'obésité. L'activité du TABr a le potentiel d'influencer considérablement le poids corporel et le métabolisme glucidique et lipidique. Ce tissu contribue à dissiper l'énergie sous forme de chaleur par l'entremise d'une protéine spéciale appelée UCP1, située sur la membrane interne des mitochondries. Les adipocytes bruns semblent être responsables d'une grande production de chaleur, considérablement plus élevée que dans d'autres organes, augmentant par le fait même la dépense énergétique corporelle. Plusieurs activateurs ont été associés au brunissement des TAB, comme l'exposition au froid, l'exercice, les hormones thyroïdiennes, les catécholamines, la capsicine, etc. La conversion du TAB en tissu adipeux beige est une nouvelle cible thérapeutique potentielle pour le traitement de l'obésité.
Les tissus adipeux expriment les deux récepteurs des cannabinoïdes, dont l'activation influence considérablement l'activité métabolique des cellules adipeuses. Il a été montré que le blocage du récepteur CB1 induit la différenciation des adipocytes blancs en un phénotype cellulaire brun thermogène, ce qui est très bénéfique lorsque l'on souhaite réduire les tissus adipeux. Les effets du récepteur CB2 sur l'obésité ont été peu caractérisés; nous savons cependant qu'il participe activement à l'homéostasie énergétique. Il a été montré que l'activation du CB2 induit une production de chaleur entraînant une dépense énergétique conséquente dans les tissus adipeux, et que la stimulation chronique du CB2 atténue la prise de poids corporel. Ainsi, le récepteur CB2 semble être une cible prometteuse dans le traitement de l'obésité puisqu'il devrait faciliter les effets anti-obésité sans provoquer d'activité psychotrope centrale.
Tétrahydrocannabinol (THC)
Le THC est un agoniste partiel à la fois des récepteurs CB1 et CB2. Il est le composant psychotrope du cannabis en raison de sa liaison au récepteur CB1 dans le cerveau. De plus, le THC active les récepteurs CB1 situés dans les régions limbique (hausse des propriétés motivationnelles de la nourriture) et hypothalamique (augmentation de l'appétit) du cerveau, ce qui entraîne une stimulation élevée de l'appétit ou les effets orexigènes, comme on les appelle. D'un autre côté, le THC s'est révélé avoir des effets potentiels pour contrer l'obésité. Dans un modèle in vivo, des chercheurs ont montré qu'une administration chronique de THC à des souris présentant une obésité liée au régime alimentaire pendant 3 et 4 semaines a évité une prise de poids causée par la réduction de l'apport énergétique. Le THC semble aussi avoir eu un effet bénéfique sur la régulation de la sensibilité à l'insuline dans les adipocytes insulinorésistants. Le mécanisme de ce double effet demeure partiellement inconnu, mais puisque le THC n'entraîne pas une stimulation maximale des récepteurs CB1, l'une des explications possibles est que les effets anti-obésité observés découleraient du fait qu'il empêche un plein agoniste, l'anandamide, de se lier au récepteur CB1, particulièrement, étant donné que les personnes obèses présentent un tonus endocannabinoïde élevé. Toutefois, l'influence positive potentielle du THC dans la prévention et le traitement de l'obésité nécessite de plus amples recherches.
Tétrahydrocannabivarine (THCV)
La THCV se lie aux récepteurs des cannabinoïdes CB1 et CB2. Son action semble varier en fonction de la dose, car elle agit comme antagoniste neutre à faible dose et comme agoniste à dose élevée des récepteurs CB1 et CB2. Vu son action antagoniste sur le CB1, la THCV apparaissait comme une candidate prometteuse dans le traitement des troubles métaboliques et de l'obésité. Cela a été partiellement confirmé par la recherche, car la THCV a montré un effet thérapeutique potentiel dans le traitement du diabète lié à l'obésité. La THCV a augmenté la sensibilité à l'insuline et a amélioré la tolérance au glucose chez des souris présentant une obésité liée au régime alimentaire ainsi que chez des souris génétiquement obèses. La THCV a aussi restauré la voie de signalisation intracellulaire de l'insuline et a diminué l'accumulation de lipides dans le foie et les adipocytes. Une étude pilote menée auprès de patients atteints de diabète de type 2 a montré que la THCV a réduit le glucose plasmatique à jeun en améliorant en parallèle la fonction des cellules bêta du pancréas. Ce phytocannabinoïde devrait donc être fortement envisagé lorsqu'un traitement des troubles métaboliques s'avère nécessaire.
Cannabidiol (CBD)
Le CBD a un vaste éventail d'effets pharmacologiques bien étudiés qui agissent par différents mécanismes. Il est un modulateur allostérique négatif du récepteur CB1, bloquant la liaison d'agonistes forts tels que l'anandamide et entraînant ainsi des effets anti-obésité. Puisque le SEC est hyperactif en cas d'obésité, on retrouve un excédent d'anandamide et de 2-AG qui provoquent la suractivation du récepteur CB1. Quant au récepteur CB2, le CBD peut agir en tant qu'agoniste ou agoniste inverse, selon la dose et le modèle de recherche. Le CBD présente aussi des affinités avec d'autres récepteurs, dont le GPR55, les adrénorécepteurs alpha-1, le 5-HT1A (sérotonine), les canaux du TRPV et le PPAR gamma. Le CBD affiche de nombreuses propriétés thérapeutiques, notamment anti-inflammatoires, antioxydantes, antinéoplasiques et anticonvulsivantes, ainsi que des effets neuroprotecteurs. Pour ces raisons, le CBD se taille une place comme agent thérapeutique potentiel pouvant être utilisé dans le traitement du diabète et de ses complications, de l'obésité, de l'ischémie, des maladies neurodégénératives ainsi que dans le soulagement de la douleur et la dépression. Comme l'obésité est accompagnée d'une inflammation chronique de faible intensité, le CBD pourrait jouer un rôle crucial dans la diminution de cette réponse inflammatoire et contribuer à l'atteinte d'une masse corporelle plus saine. Le CBD a été étudié en profondeur à cet égard et il s'est avéré rehausser le niveau de glutathion (GSH), d'adénosine triphosphate (ATP) et de nicotinamide adénine dinucléotide (NAD) ainsi qu'augmenter la lipolyse intracellulaire et l'activité mitochondriale (36). Le CBD a de nombreux bienfaits sur le foie, un organe essentiel à tous les processus métaboliques et à l'équilibre énergétique, car il atténue la stéatose hépatique (réduction des triglycérides et accumulation de gouttelettes de graisses), la réponse inflammatoire, le stress nitrosatif, la réduction de la peroxydation lipidique, l'expression des espèces réactives de l'oxygène et l'infiltration des neutrophiles dans le foie. Les effets du CBD sur la prise et les préférences alimentaires, de même que sur la prise de poids, demeurent ambigus et montrent une gamme de résultats déconcertants. Une étude a conclu que le CBD a entraîné une réduction de la prise de poids corporel chez des rats, tandis que d'autres n'ont montré aucun effet significatif sur la prise alimentaire et le poids corporel chez des souris et des rats. Une étude a aussi révélé que chez les rats suivant un régime alimentaire riche en gras, le CBD a entraîné une augmentation du poids corporel, malgré une importante réduction de la prise alimentaire. Peu importe les résultats contradictoires du CBD sur l'alimentation, celui-ci montre de multiples effets bénéfiques sur une vaste gamme de changements et de pathologies qui accompagnent l'obésité. Puisqu'il se lie à de nombreux récepteurs, il agit sur beaucoup d'organes essentiels au métabolisme comme le foie, les tissus adipeux, le pancréas et le cœur. Il est intéressant de noter qu'il entraîne des changements désirables aux hormones intestinales, telles que le peptide insulinotrope dépendant du glucose (GIP) et les concentrations d'adipokines.

Source de la photo : Bielawiec et coll., 2020
| CBD | |||
| CB1, CB2 | TRPV | GPR55 | |
| Tissus | |||
| Foie | Cœur | Tissu adipeux | Pancréas endocrine |
| ↑ lipolyse | ↓ fibrose cardiaque | ↑ lipolyse | ↑ dépense énergétique |
| ↑ activité mitochondriale | ↓ stress oxydatif | ↑ absorption du glucose | ↓ TNF alpha, INF gamma, COX |
| ↑ AMPKa2 | ↓ inflammation | ↑ activité mitochondriale | ↑ NO, PGE2 |
| ↑ ERK1/2 | ↓ mort cellulaire | ↑ PGC-1 alpha, PPAR gamma | ↑ IL-4, IL-10 |
| ↑ STAT | |||
Conclusion
Les comorbidités liées à l'obésité sont en croissance et sont lourdes de conséquences pour la société, en plus de réduire la qualité de vie des patients. De récentes découvertes dans le domaine du brunissement du tissu adipeux blanc (transformation de TAB à TABr) ont soulevé le rôle possible de ce phénomène dans le traitement de l'obésité. On a établi un lien entre l'activité du TABr et une amélioration du profil métabolique chez des adultes. L'activation du CB2 accroît le brunissement et la transformation d'énergie chimique en énergie thermique, ce qui pourrait représenter un morceau important du casse-tête.
Il est aussi important de cibler le CB1, tout en gardant à l'esprit les expériences avec le Rimonabant, un antagoniste du récepteur CB1 qui semblait être un médicament prometteur contre l'obésité lors des essais cliniques, mais qui s'est avéré avoir d'énormes effets secondaires psychiatriques et a donc dû être retiré du marché. L'interruption d'un essai clinique portant sur un inhibiteur de l'hydrolase des amides d'acides gras (FAAH) en raison de la survenue d'effets secondaires graves a aussi montré qu'il faut faire preuve de grande précaution lorsqu'on manipule ce système de protection fondamental et vital. Là encore, les phytocannabinoïdes et d'autres ligands des récepteurs cannabinoïdes issus du monde végétal laissent voir un immense potentiel. L'objectif consiste à trouver des antagonistes du récepteur CB1 et des agonistes du récepteur CB2 dans le monde végétal. Ils montrent un profil d'innocuité élevé et des effets secondaires négligeables, en plus d'avoir de multiples cibles dans l'endocannabinoïdome qui favorisent la santé du métabolisme, la dépense énergétique, l'homéostasie biochimique et le bien-être émotionnel.
Documentation
Jung SM, Sanchez-Gurmaches J, Guertin DA. Brown Adipose Tissue Development and Metabolism. Handb Exp Pharmacol. 2019;251:3-36. doi: 10.1007/164_2018_168. PMID: 30203328; PMCID: PMC7330484.
Bielawiec P, Harasim-Symbor E, Chabowski A. Phytocannabinoids: Useful Drugs for the Treatment of Obesity? Special Focus on Cannabidiol. Front Endocrinol (Lausanne). 2020 Mar 4;11:114. doi: 10.3389/fendo.2020.00114. PMID: 32194509; PMCID: PMC7064444.
Rossi F, Punzo F, Umano GR, Argenziano M, Miraglia Del Giudice E. Role of Cannabinoids in Obesity. Int J Mol Sci. 2018 Sep 10;19(9):2690. doi: 10.3390/ijms19092690. PMID: 30201891; PMCID: PMC6163475.
Borowska M, Czarnywojtek A, Sawicka-Gutaj N, Woliński K, Płazińska MT, Mikołajczak P, Ruchała M. The effects of cannabinoids on the endocrine system. Endokrynol Pol. 2018;69(6):705-719. doi: 10.5603/EP.a2018.0072. PMID: 30618031.
Kaur R, Ambwani SR, Singh S. Endocannabinoid System: A Multi-Facet Therapeutic Target. Curr Clin Pharmacol. 2016;11(2):110-7. doi: 10.2174/1574884711666160418105339. PMID: 27086601.
Behl T, Chadha S, Sachdeva M, Sehgal A, Kumar A, Dhruv, Venkatachalam T, Hafeez A, Aleya L, Arora S, Batiha GE, Nijhawan P, Bungau S. Understanding the possible role of endocannabinoid system in obesity. Prostaglandins Other Lipid Mediat. 2021 Feb;152:106520. doi: 10.1016/j.prostaglandins.2020.106520. Epub 2020 Nov 26. PMID: 33249225.
Abioye A, Ayodele O, Marinkovic A, Patidar R, Akinwekomi A, Sanyaolu A. Δ9-Tetrahydrocannabivarin (THCV): a commentary on potential therapeutic benefit for the management of obesity and diabetes. J Cannabis Res. 2020 Jan 31;2(1):6. doi: 10.1186/s42238-020-0016-7. PMID: 33526143; PMCID: PMC7819335.